Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC

Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC
Připomeňte si předchozí díly z této zajímavé série:
- První díl: Úvod do validace čištění: principy, rizika a regulační požadavky
- Druhý díl: Volba analytických metod při validaci čištění: TOC vs. HPLC vs. další techniky
- Třetí díl: TOC při validaci čištění: principy, osvědčené postupy a časté chyby
- Čtvrtý díl: Validace metod TOC: Zajištění robustnosti, citlivosti a souladu s předpisy
Stanovení vědecky obhajitelných limitů reziduí představuje základní pilíř farmaceutické validace čištění. Přístup založený na řízení rizik a datech podložená akceptační kritéria chrání nejen soulad s regulačními požadavky, ale především bezpečnost pacientů a integritu produktu.
Tento článek poskytuje praktické vodítko pro výpočet, zdůvodnění a aplikaci robustních limitů validace čištění se zvláštním důrazem na analýzu celkového organického uhlíku (TOC). Veškeré postupy a doporučení vycházejí z dokumentu z roku 2021 „Guidance on Aspects of Cleaning Validation in Active Pharmaceutical Ingredient Plants“ vydaného výborem Active Pharmaceutical Ingredients Committee (APIC), revize duben 2019, aktualizace únor 2021 (dále jen APIC Cleaning Validation Guidance). APIC je sektorovou skupinou Evropské rady chemického průmyslu (CEFIC), sdružuje odborníky z praxe a je celosvětově uznáván pro tvorbu prakticky orientovaných, vědecky podložených doporučení pro validaci čištění a zajištění souladu s požadavky GMP.
Hierarchie APIC při stanovování akceptačních kritérií
APIC Cleaning Validation Guidance upřednostňuje při stanovení maximálního přípustného přenosu (MACO, Maximum Allowable Carry Over) zdravotně odvozené limity expozice (PDE/ADE). Pokud tyto limity nelze stanovit, je možné použít odůvodněné alternativy, například toxikologické, terapeutické nebo obecné limity (např. 10 ppm, 100 ppm), za předpokladu vědeckého zdůvodnění a interního schválení.
Klíčový princip (APIC Cleaning Validation Guidance, oddíl 4.1 a 4.2):
„Akceptační kritéria by měla být přednostně založena na výpočtech Acceptable Daily Exposure (ADE, přijatelná denní expozice) nebo Permitted Daily Exposure (PDE, povolená denní expozice), pokud jsou tato data k dispozici.“
„Pokud jsou výsledky výpočtu MACO méně přísné nebo nejsou k dispozici toxikologická data pro meziprodukty, může být vhodné použít obecný limit… Hodnota zvolená jako interní horní limit musí být zdůvodněna a musí odpovídat typu chemické látky nebo skupiny látek (např. 10 ppm, 100 ppm).“ (str. 12)
Osvědčený postup:
MACO by měl být vždy vypočten všemi relevantními a zdůvodněnými přístupy, tedy na základě zdravotně odvozených limitů expozice (PDE/ADE), terapeutických kritérií, toxikologických údajů a (pokud je to relevantní) obecných limitů. Akceptační kritérium pro validaci čištění musí být stanoveno jako nejnižší (nejpřísnější) hodnota získaná z výpočtů, aby byla zajištěna skutečná „worst-case“ ochrana a soulad s požadavky APIC.
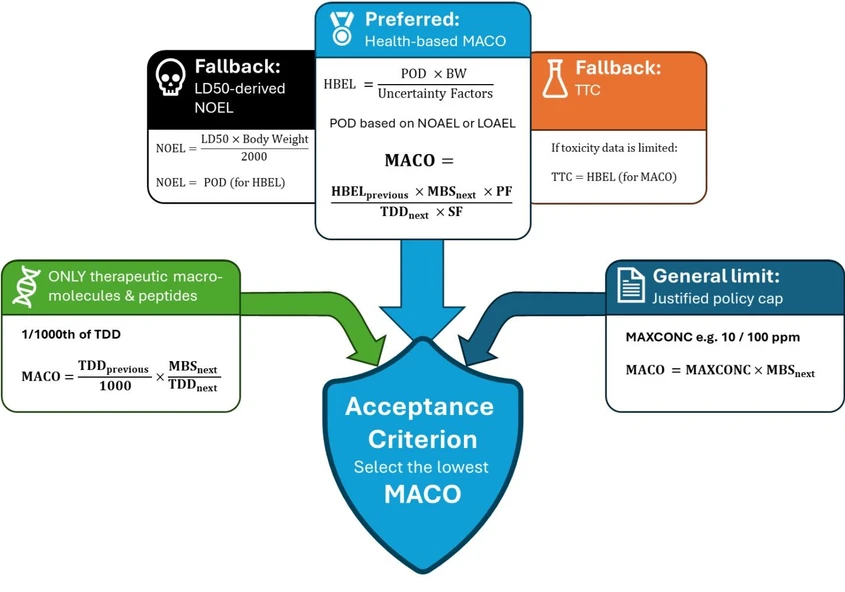 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Tento diagram shrnuje tři paralelní přístupy ke stanovení MACO schválené dokumentem APIC („limit založený na zdravotním hodnocení“, „1/1000 TDD pro makromolekuly/peptidy“ a „obecný limit“), včetně příslušných výpočtových vzorců a klíčové logiky jejich použití. Metoda, která vede k nejnižší hodnotě, musí být v souladu s požadavky APIC Guidance 2021 zvolena jako akceptační kritérium pro validaci čištění (worst case).
Vzorec pro výpočet MACO: základ všech přístupů
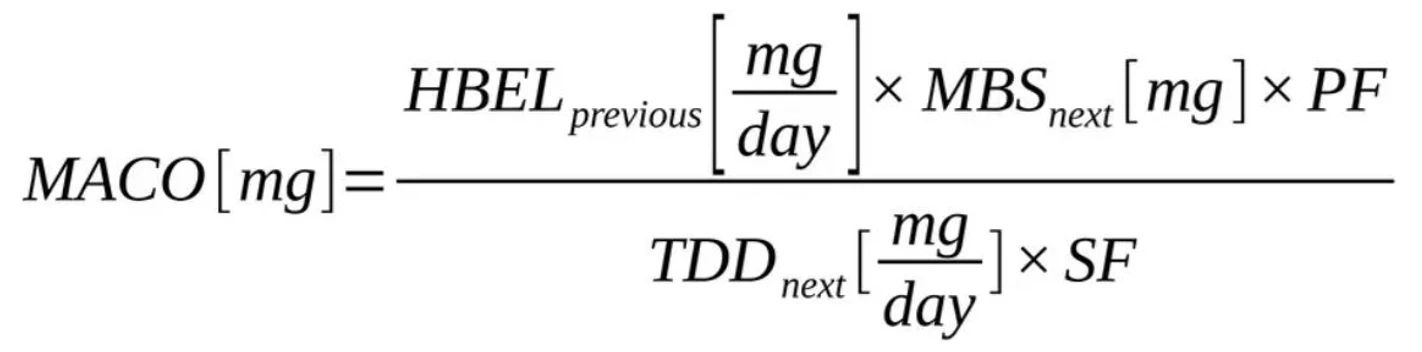 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Kde:
- MACO: Maximální přípustný přenos
- HBEL (PDE/ADE): Zdravotně odvozený limit expozice pro předchozí látku
- MBSnext: Minimální velikost šarže následujícího produktu
- PF: Purging faktor (výchozí hodnota = 1; upravuje se na základě procesních dat)
- TDDnext: Maximální terapeutická denní dávka následujícího produktu
- SF: Faktor bezpečnosti (výchozí hodnota = 1, pokud nejsou přítomna specifická rizika pro pacienta; stanovuje toxikolog)
Proč je minimální velikost šarže klíčová
Ve všech výpočtech MACO vždy vycházejte z minimální velikosti šarže následujícího vyráběného produktu – nikoli z nominálního či maximálního objemu zařízení. Tento princip je základním kamenem přístupu založeného na řízení rizik a scénáři „worst case“ podle pokynů APIC a EMA. Zajišťuje, že případná přítomná rezidua budou při zpracování nejmenší možné šarže nejvíce koncentrována (a tedy představují nejvyšší potenciální riziko). Použití minimální velikosti šarže proto vždy vede ke konzervativnějšímu, z hlediska pacienta bezpečnějšímu akceptačnímu kritériu, plně v souladu s regulačními požadavky (APIC Cleaning Validation Guidance, část 4.2.1).
1. Zdravotně odvozená data: preference PDE/ADE (HBEL)
U většiny přípravků se MACO stanovuje na základě zdravotně odvozených limitů expozice (HBEL) v souladu s pokyny APIC a EMA. Tento limit expozice, označovaný jako PDE (Permitted Daily Exposure) nebo ADE (Acceptable Daily Exposure), stanovují toxikologové na základě dat ze studií na zvířatech i u lidí. Při jeho určování je vždy uplatňován přístup založený na řízení rizik a principu „worst case“
Hlavní vzorec pro HBEL (standardní POD)
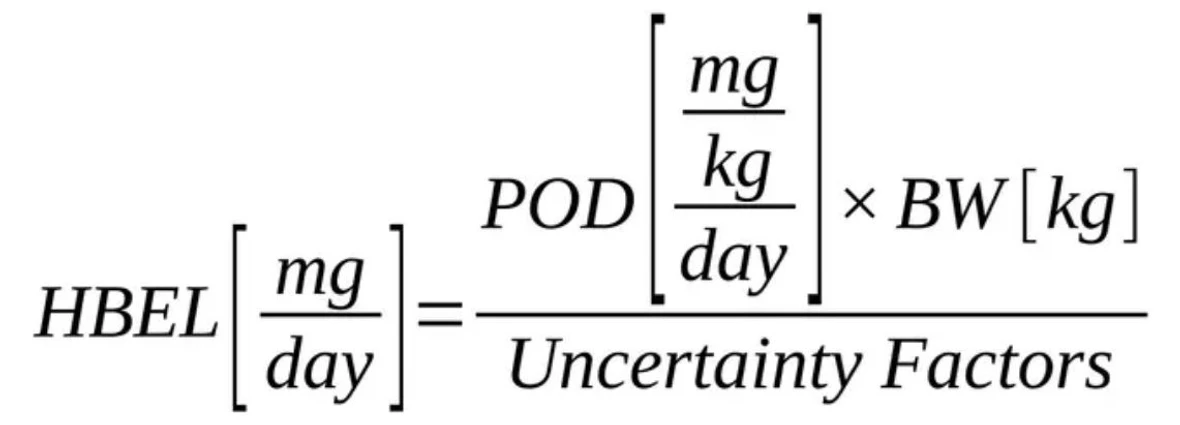 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Kde:
- HBEL (Health-Based Exposure Limit): Vypočtená hodnota představující maximální bezpečnou denní expozici, která slouží jako vstupní parametr pro výpočet MACO. HBEL je rovněž označován jako Permitted Daily Exposure (PDE) nebo Acceptable Daily Exposure (ADE) – všechny tyto pojmy označují stejný zdravotně odvozený limit expozice, stanovený na základě POD, tělesné hmotnosti a souboru faktorů nejistoty, a jsou v rámci validace čištění podle APIC a EMA používány zaměnitelně.
- POD (Point of Departure): Výchozí toxikologická hodnota. Nejčastěji NOAEL (No Observed Adverse Effect Level: nejvyšší testovaná dávka bez pozorovaného nepříznivého účinku), případně, pokud není k dispozici, LOAEL (Lowest Observed Adverse Effect Level: nejnižší testovaná dávka s pozorovaným nepříznivým účinkem). Pokud není k dispozici ani jedna z těchto hodnot, lze POD odhadnout z hodnoty LD50 (viz oddíl 3) nebo jako krajní možnost použít přístup TTC.
- BW (Body Weight): Obvykle 50 kg pro dospělou osobu; zvoleno jako konzervativní regulatorní bezpečnostní standard.
- Uncertainty Factors: Souhrnný násobící faktor zohledňující mezidruhové rozdíly, variabilitu mezi jednotlivci, extrapolaci délky studie na celoživotní expozici, úplnost dostupných dat a závažnost účinku. Výchozí hodnoty a postupy výpočtu jsou podrobně popsány v pokynu EMA pro stanovení zdravotně odvozených limitů expozice (EMA/CHMP/CVMP/SWP/169430/2012) a v pokynech ICH. Toxikolog může na základě dostupných dat a posouzení rizika zdůvodnit jejich úpravu.
Pro další informace viz APIC Cleaning Validation Guidance (2021), str. 9, a EMA/CHMP/CVMP/SWP/169430/2012, oddíl 4.1.
2. Použití obecného limitu (10 ppm, 100 ppm apod.)
Pokud nejsou k dispozici toxikologická nebo farmakologická data, případně pokud vypočtené hodnoty MACO nejsou dostatečně přísné, APIC umožňuje stanovit vědecky zdůvodněný obecný horní limit, například 10 ppm, 100 ppm nebo jinou hodnotu odpovídající dané chemické třídě a interní politice společnosti:
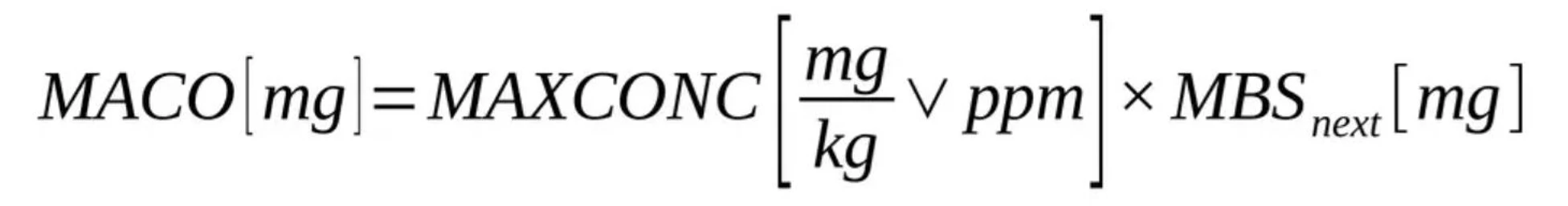 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Kde:
- MAXCONC: Obecný limit maximální přípustné koncentrace předchozí látky v následující šarži
- MBSnext: Minimální velikost šarže následujícího produktu
Obecný horní limit maximální koncentrace kontaminující látky v následující šarži (MAXCONC) se obvykle pohybuje v rozmezí 5–500 ppm (běžně 100 ppm pro API a 10 ppm pro léčivé přípravky). Zvolená hodnota musí být vědecky nebo historicky zdůvodněna (APIC Cleaning Validation Guidance, str. 12).
Pokud interní politika společnosti stanoví úroveň typu „not to exceed“ (např. 10 ppm), musí být vypočtené hodnoty MACO převyšující tento limit omezeny na tuto hodnotu.
Kdy a jak použít obecný limit
Obecný limit by měl být použit pouze v případě, že nelze stanovit zdravotně podložené nebo toxikologické limity, nebo pokud výsledky výpočtu MACO nejsou přísnější než interně stanovená hodnota. APIC uvádí, že tento přístup je nejvhodnější zejména pro procesní meziprodukty nebo chemické látky, u nichž nemusí být k dispozici data o bezpečnosti pro pacienty. U API a dalších dobře charakterizovaných látek je vždy vhodné upřednostnit limity založené na vědeckých datech.
Při použití obecného limitu je vždy nutné:
- Jasně zdokumentovat vědecké nebo interní odůvodnění,
- Vztáhnout zvolenou hodnotu k rizikovému profilu dané látky nebo příslušné třídě,
- Zdůvodnit její použití absencí robustnějších dat,
- A zaznamenat ji jako vědomou, řízenou výjimku na základě posouzení rizika – nikoli jako výchozí zjednodušený postup.
APIC uvádí: „Hodnota zvolená jako interní horní limit musí být zdůvodněna a musí odpovídat typu chemické látky nebo skupiny látek …“ (str. 12)
3. Další přístupy: terapeutická dávka, toxikologická data a TTC
Pokud nelze zdravotně odvozené limity (PDE/ADE) stanovit na základě robustních klinických nebo chronických toxikologických dat, APIC umožňuje následující náhradní výpočetní přístupy, z nichž každý má specifické požadavky a vyžaduje vědecké zdůvodnění:
Terapeutická dávka (1/1000 TDD)
- Pro terapeutické makromolekuly, peptidy nebo v odůvodněných případech. APIC doporučuje tento přístup zejména pro proteiny a peptidy, a to z důvodu jejich spolehlivé degradace/inaktivace za podmínek čištění (extrémní pH a/nebo teplo). Faktor 1/1000 poskytuje bezpečnostní rezervu zajišťující ochranu pacienta i v případě možného přenosu intaktní látky (APIC Cleaning Validation Guidance, oddíl 4.2.3).
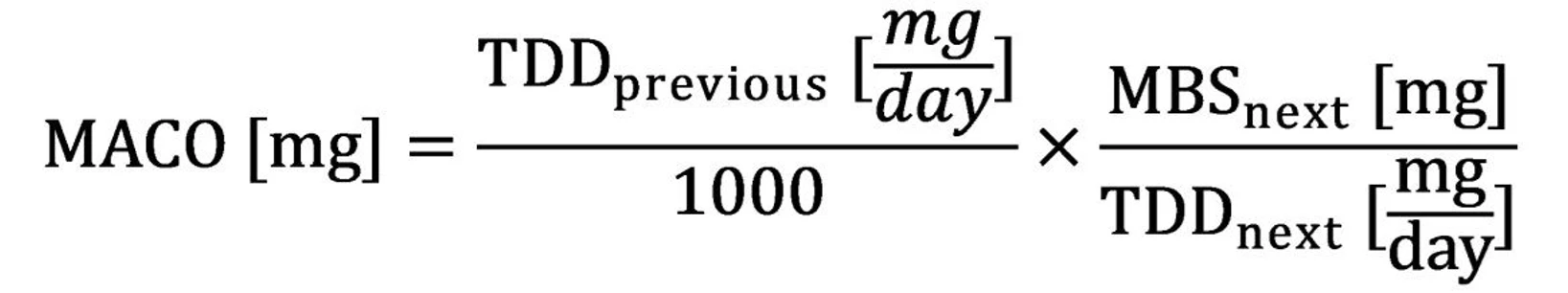 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Poznámka: Matematicky je tento postup totožný s použitím vzorce MACO s bezpečnostním faktorem (SF) 1000. Není určen pro nízkomolekulární API.
Toxikologická data (odvozená z LD50)
- Pokud nelze stanovit primární POD (NOEL/NOAEL), APIC a EMA umožňují odhadnout POD na základě dostupných údajů LD50.
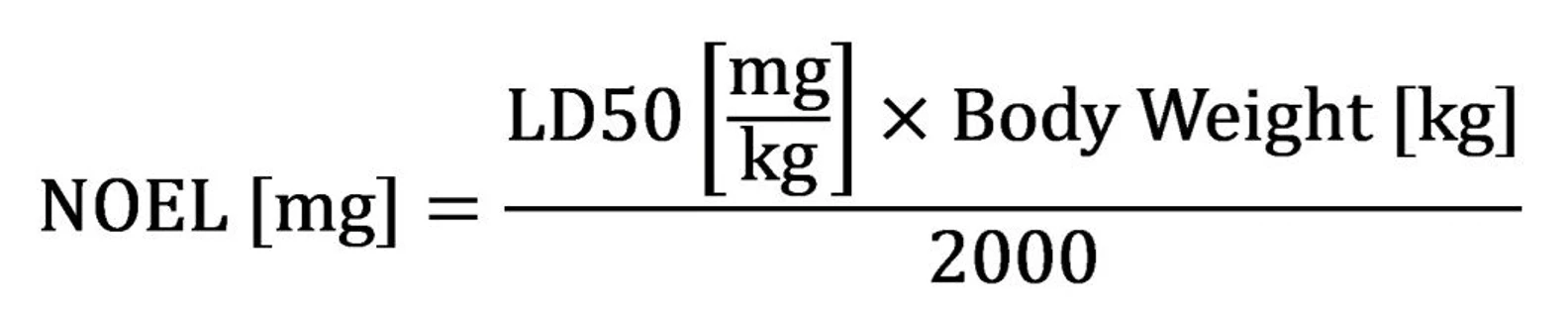 Shimadzu - Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC 6.jpg
Shimadzu - Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC 6.jpg
Tím se získá hodnota v [mg], představující NOEL odvozený pro standardní tělesnou hmotnost (obvykle 50 kg), která se přímo použije jako HBEL [mg/den] ve vzorci MACO. Je nutné aplikovat vyšší faktory nejistoty; tento přístup by měl být použit pouze jako krajní možnost, při plném zdůvodnění a dokumentaci.
TTC (Threshold of Toxicological Concern)
- Pokud jsou k dispozici pouze obecná toxikologická data na úrovni tříd látek, poskytuje TTC konzervativní výchozí prahovou hodnotu denního příjmu (např. 1,5 µg/den pro genotoxické látky, 10–100 µg/den pro ostatní). Prahová hodnota TTC (v [mg/den], např. 0,0015 mg/den pro genotoxické látky) se použije jako HBEL v obecném vzorci MACO.
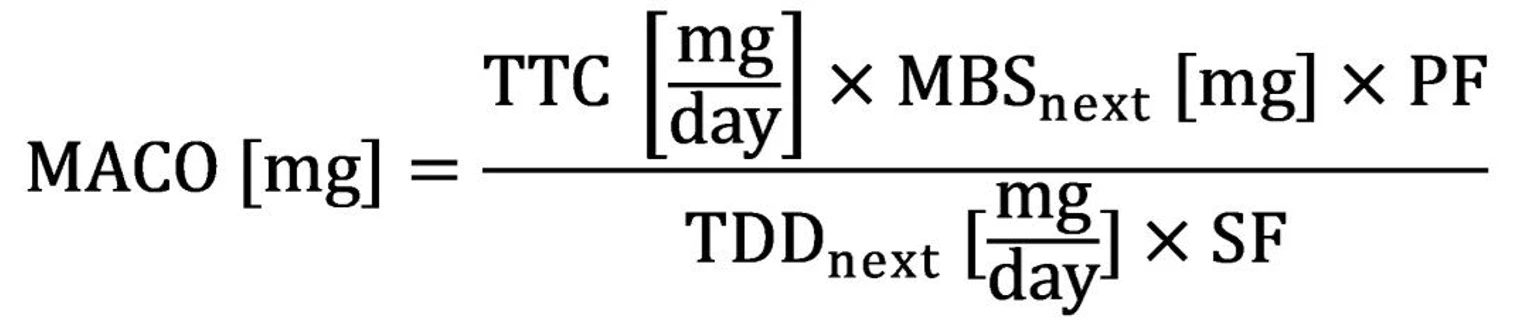 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Zvolte prahovou hodnotu TTC podle příslušné třídy látky a celý postup plně zdokumentujte a zdůvodněte v souladu s APIC 2021.
Požadavek APIC:
Vždy používejte nejspolehlivější a vědecky zdůvodněná dostupná data. Pokud jsou použity náhradní nebo odhadové přístupy, musí být zdokumentována logika výpočtu, volba POD, všechny bezpečnostní a nejistotní faktory a celkové zdůvodnění zvoleného postupu.
Limity pro stěry a oplachy: výpočet v souladu s APIC
Akceptační kritérium pro oplach (na celkový vzorek)
U odběru vzorku finálního oplachu je akceptační kritérium založeno na celkovém množství reziduí získaných z celého zařízení. Změřte koncentraci ve vzorku oplachu ([mg/l] nebo [µg/l]) a následně vypočítejte celkové množství nalezeného rezidua.
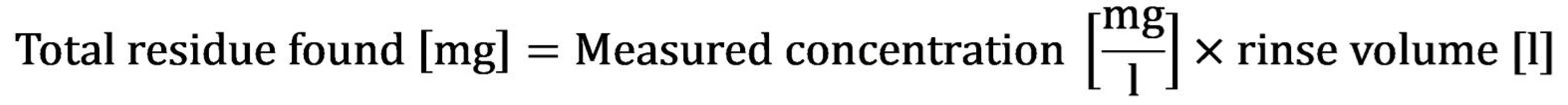 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Akceptační kritérium je splněno, pokud toto celkové množství nepřekročí vypočtenou hodnotu MACO [mg] pro čištěné zařízení nebo výrobní linku.
Nepoužívejte ani nedokumentujte cílovou hodnotu přepočtenou na litr oplachu, pokud váš postup nestanoví pevně definovaný objem oplachu; rozhodujícím kritériem je vždy celkové získané množství rezidua.
Akceptační kritérium pro stěr (na jednotku plochy)
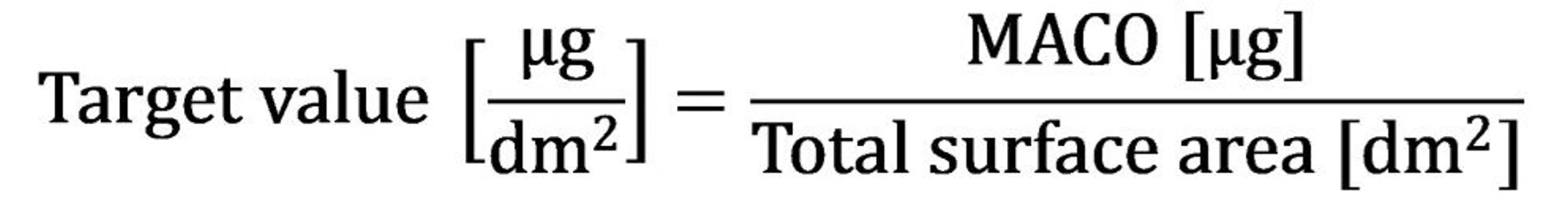 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Každý výsledek stěru (bez ohledu na velikost odebrané plochy) se přepočítá na jednotku plochy [dm²] a porovná se s příslušným akceptačním limitem.
Více stěrů (požadavky APIC):
Při odběru stěrů z více míst zařízení (např. z různých částí výrobní linky nebo z míst představujících „worst case“):
- Každý jednotlivý výsledek stěru přepočtený na jednotku plochy (mg nebo µg/dm²) nesmí překročit stanovený limit na plochu.
- Součet všech reziduí ze všech stěrů (včetně případných korekcí na výtěžnost nebo plochu) nesmí překročit hodnotu MACO pro dané zařízení.
- Pro splnění požadavků APIC jsou vyžadovány obě tyto kontroly (viz Guidance, str. 15), aby byla zajištěna regulatorní i vědecká robustnost bez ohledu na to, zda je vzorkováno jedno nebo více míst.
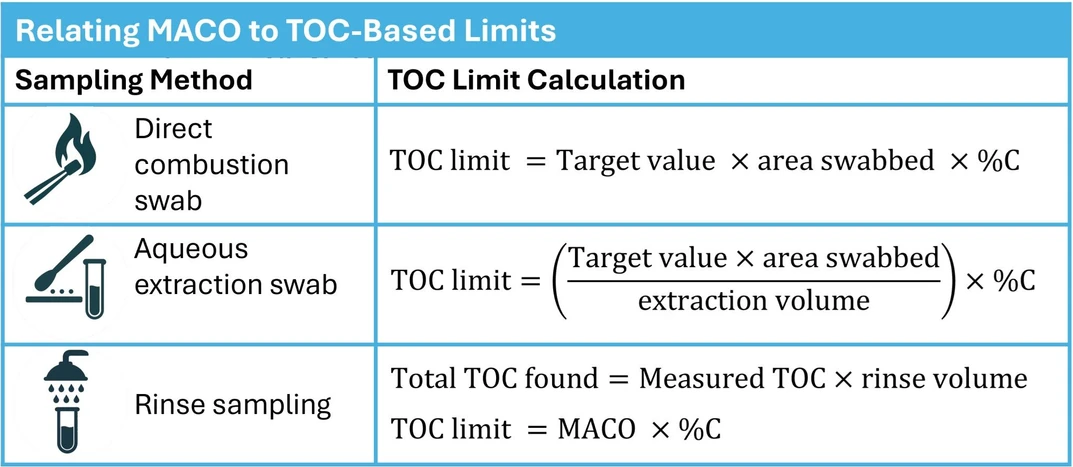
Vztah mezi MACO a limity založenými na TOC: role techniky odběru vzorků
 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Při použití analýzy TOC pro validaci čištění zajistěte, aby akceptační kritéria odvozená z MACO („cílová hodnota“) a vaše výsledky měření TOC byly přímo porovnatelné v závislosti na zvoleném protokolu odběru vzorků.
Více informací o měření TOC a technikách odběru vzorků naleznete ve 3. dílu.
Přímé spalování stěru
Analyzátor pevných vzorků TOC udává množství uhlíku (mg nebo µg) ve stěru po přímém spalování. Tento absolutní výsledek TOC (mg C na stěr) porovnejte s příslušným limitem.
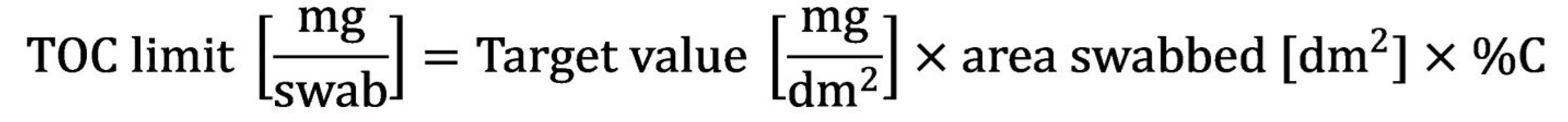 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Porovnejte hodnotu TOC na stěr s tímto limitem.
Stěr s následnou vodnou extrakcí
Po extrakci stěru do známého objemu přístroj udává TOC v jednotkách mg/l (nebo µg/l).
Výpočet:
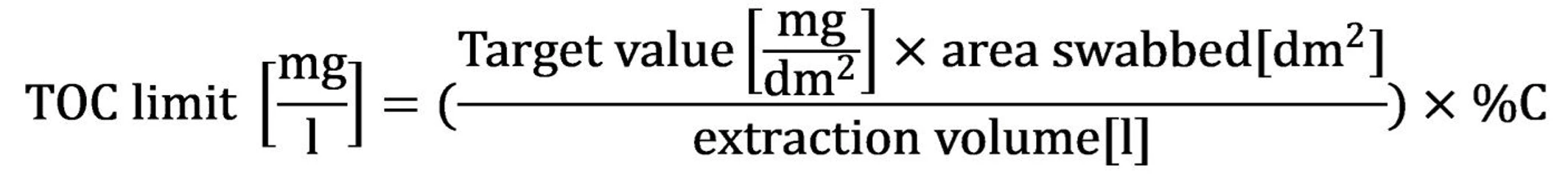 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Naměřenou koncentraci TOC v extrakčním roztoku přímo porovnejte s příslušnou limitní hodnotou.
Odběr vzorku oplachu pro TOC
U oplachu vždy vypočítejte celkové množství nalezeného TOC:
 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Tuto celkovou hodnotu přímo porovnejte s akceptačním limitem TOC:
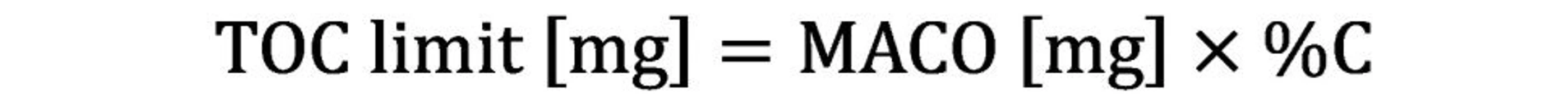 Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Shimadzu: Stanovení obhajitelných limitů při validaci čištění – MACO, zdravotní kritéria a osvědčené postupy pro TOC.
Splnění požadavku je založeno výhradně na tom, zda celkové množství nalezeného TOC nepřekročí limit stanovený pro danou šarži.
Vždy ověřte, že vypočtený limit TOC — jak z hlediska jednotek, tak logiky výpočtu — odpovídá použitému přístroji a analytickému postupu.
Dokumentace a zdůvodnění
Pro skutečný soulad s požadavky a auditovatelnost:
- Veškeré výpočty, zvolené metody a rozhodnutí musí být plně transparentně zdokumentovány v protokolech a zprávách.
- Uveďte zdroje expozičních limitů, velikostí šarží a zdůvodnění použití jakéhokoli obecného limitu nebo náhradního postupu.
- V každé fázi rozhodování jasně prezentujte použité jednotky, logiku výpočtu a odborné zdůvodnění.
Shrnutí
APIC Cleaning Validation Guidance stanovuje jasný, vědecky podložený postup:
- Pokud je to možné, používejte zdravotně odvozené expoziční limity.
- K terapeutickým, toxikologickým nebo interně stanoveným obecným limitům přistupujte pouze jako k odůvodněné alternativě.
- Akceptační limit pro stěry stanovte jako hodnotu vztaženou na jednotku plochy (MACO dělené celkovou plochou zařízení) a každý jednotlivý výsledek posuzujte vůči tomuto limitu.
- Při více stěrech kontrolujte jak jednotlivé výsledky přepočtené na plochu, tak i součet všech reziduí vůči celkovému MACO.
- Každé rozhodnutí a každý výpočet musí být zdokumentovaný.
- Limity odvozené z TOC stanovujte jako nejnižší bezpečný signál uhlíku pro všechna potenciální rezidua s použitím správného, protokolem definovaného vzorce.
Závěrečná poznámka
Tento článek poskytuje přehled a praktický pracovní rámec vycházející z APIC Cleaning Validation Guidance. Pro reálnou implementaci, regulatorní inspekce nebo nestandardní situace vždy prostudujte úplné znění pokynů, které obsahuje detailní technické informace a specifické požadavky podle kontextu použití.
Specifické situace, jako je pokročilé seskupování produktů (bracketing), volba úrovně čištění nebo detailní součty celkového přenosu, jsou podrobně rozpracovány v oddílech 4.2.4, 5.0, 7.4/7.5 a 8.3 dokumentu APIC.
🔎 Zvažujete možnosti analyzátoru TOC? Podívejte se blíže na TOC-L!
- Guidance on Aspects of Cleaning Validation in Active Pharmaceutical Ingredient Plants (APIC, CEFIC, Revision April 2019, updated February 2021), esp. Sections 4.1-4.2, pp. 8-14.
- Guideline on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities (EMA/CHMP/CVMP/SWP/169430/2012)




